| year | act | event |
| 1989 | Joshua S. BogerとKevin J. Kinsellaがケンブリッジで創業 | |
| 1991 | IPO | NASDAQに新規株式公開 |
| 1993 | collabo | プロテアーゼ阻害剤についてGSKと共同研究→Agenerase(Amprenavir) |
| 1996 | R&D | C 型肝炎ウイルスのプロテアーゼ構造を解明 |
| 1997 | collabo | キナーゼ阻害剤についてキッセイ薬品と共同研究 |
| 1999 | FDA | HIVプロテアーゼ阻害薬Agenerase(Amprenavir) 承認 |
| 2001 | M&A | Aurora Biosciences Corporation :6億ドル |
| 2003 | FDA | HIVプロテアーゼ阻害薬Lexiva(Fosamprenavir)承認 |
| 2005 | R&D | 嚢胞性線維症治療薬候補Ivacaftor発見 |
| 2011 | FDA | C型肝炎治療薬プロテアーゼ阻害剤Incivek (テラプレビル:和名テラビック) 承認 |
| 2012 | FDA | 嚢胞性線維症治療薬kalydeco(Ivacaftor) 承認 |
| 2014 | 本社をケンブリッジからボストンへ移転 | |
| 2015 | FDA | 嚢胞性線維症治療薬Orkambi(ivacaftor/ lumacaftor)承認 |
| collabo | CRISPR Therapeuticsと遺伝子編集技術に焦点を当てた共同研究 | |
| 2016 | collabo | Modernaと嚢胞性線維症治療のためのmRNA治療薬を共同研究 |
| 2018 | FDA | 嚢胞性線維症治療薬Symdeko(ivacaftor/tezacaftor and ivacaftor)承認 |
| 2019 | FDA | 嚢胞性線維症治療薬Trikafta(elexacaftor/tezacaftor/ivacaftor)承認 |
| M&A | Semma Therapeuticsを9.5億ドル→一型糖尿病細胞療法の促進目的 | |
| M&A | Exonics Therapeuticsを10億ドル→筋ジストロフィー治療薬候補 | |
| 2020 | collabo | Affinia TherapeuticsのAAVカプシド技術を使い遺伝子治療の共同研究 |
| 2021 | collabo | Obsidian TherapeuticsのcytoDRiVE技術を使い遺伝子編集の共同研究 |
| 2022 | M&A | ViaCyteを3.2億ドル 買収目的:一型糖尿病治療VX-880の開発促進技術 |
創業から嚢胞性線維症治療薬の発見まで
Vertex Pharmaceuticals(VRTX)はアメリカ合衆国ボストンを拠点とする製薬会社。
1989年創業とまだ社歴30年ちょっとだが時価総額は既に10兆円を超え日本のどの製薬会社よりも大きい。
創業者はアメリカの製薬最大手メルクで研究者だったJoshua S. BogerとKevin J. Kinsellaの2人。メルクで研究していたサラリーマン研究者2人が脱サラしてVertex を創業。
病気に関係するたんぱく質の構造を分子レベルで解明してその構造にアプローチできる薬を作ろうとしていたのだがそんな簡単にはいかず。
HIVプロテアーゼの結晶構造解析を成功させたまでは良かったがそのプロテアーゼを阻害するための物質がなかなか作れない。自社開発では限界があるということになり抗ウイルス薬開発に定評のある英国のGSKなどと共同開発することに。
共同開発の甲斐もあり1999年にHIVプロテアーゼ阻害薬Agenerase(Amprenavir)がやっとFDAに承認されたがGSKからの販売となりVRTXはその販売ロイヤリティだけとイマイチな結果に。
自社販売の薬であるC型肝炎治療薬Incivek (Telaprevir)は創業から20年以上経過した2011年についに完成。
| テラビック錠250mg |
 |
日本では田辺三菱製薬からテラビック錠という商品名で販売されている。いや、販売されていた。
日本初のC型肝炎ウイルス直接作用型抗ウイルス薬テラビック錠は10年もしないで世の中から消えた。副作用や飲み合わせの複雑さ、そしてライバルの製薬会社が作った薬の方が性能が良いという理由で。
長い年月を掛けて開発した薬が売れなくなると普通の創薬ベンチャーならこの時点でthe end。となるがVRTXのサクセスストーリーはここから始まる。
VRTXは2001年にサンディエゴにある小さな製薬会社Aurora Biosciences Corporationを6億ドルで買収していた。Auroraは2000年に嚢胞性線維症財団(CFF)と契約を結びCFFから3,000万ドルの投資を受けてCF薬の研究開始。
この研究が2005年にIvacaftorという最初の根本的な嚢胞性線維症治療薬の発見に繋がる。
2023年8月時点でもVRTXは嚢胞性線維症の治療薬だけを販売している。このIvacaftorが無ければ今のVRTXも無い。
嚢胞性線維症(Cystic fibrosis: CF)とは?
cystic fibrosis transmembrane conductance regulator(CFTR)の遺伝子変異が病気の根本原因。
CFTRは粘膜や上皮膜に存在する塩化物イオンチャネル。最も多い変異はNBD1に存在する508番目のフェニルアラニンが欠失した∆F508変異。
チャネルというのは通り道であり塩化物イオンの出入りを制御している。そのCFTRに遺伝的な異常が起こると塩化物イオンが通れなくなる。
塩化物イオンチャネルに作用する下剤としてアミティーザ(一般名:ルビプロストン)がある。この下剤は塩化物イオンチャネルを介して腸管の管腔側に塩化物イオンを増やしナトリウムイオンと結合させNaCl(塩)を作り浸透圧を発生させ腸管内の水分を増やす。
つまり
塩化物イオンチャネル開く→水分が出る→粘液サラサラ
塩化物イオンチャネル閉る→水分が出ない→粘液ネバネバ
粘液がネバネバになると全身で困ったことが起こる。
具体的には
- 気管支:細気管支にネバネバが発生するとそこに緑膿菌などの細菌が住み着く→呼吸不全
- 膵臓:消化酵素のタンパク濃度が高まり小膵管が閉塞→膵外分泌不全
- 腸管:水分の分泌量が低下→腸閉塞、イレウス
CFは全身性疾患なので他にも症状は現れるが上記3つは頻発。特に気管支症状はほぼ100%発症。呼吸不全はそのまま生命に直結する。なのでCFは致命的な疾患。
あと汗の塩分濃度が濃くなるという特徴がある(汗中塩化物イオン濃度60mmol/L以上)。
日本では患者総数が100人行くかどうかの超希少疾患だが有病率に人種差があり白人が多い欧米には患者がたくさんいる。
たくさんと言っても数万人だが一人当たりの年間薬剤費が20万ドル以上するので売上的に大きい。
嚢胞性線維症の治療薬
| 承認年 | 商品名 | 一般名 | ||
| 2012 | KALYDECO | Ivacaftor | ||
| 2015 | ORKAMBI | Ivacaftor | lumacaftor | |
| 2018 | SYMDEKO | Ivacaftor | tezacaftor | |
| 2019 | TRIKAFTA | Ivacaftor | tezacaftor | elexacaftor |
Ivacaftor:CFTRポテンシエーター
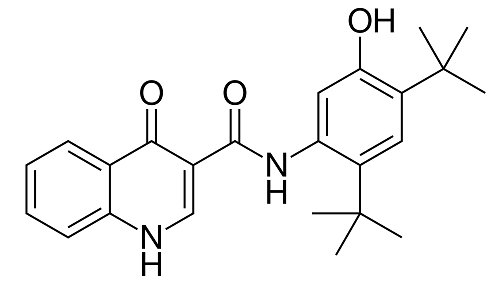
初めての根本的治療薬として2012年にFDA承認。CFTRの膜貫通領域に直接的に作用してチャネル開口状態を長引かせることによって開口確率を改善。VRTX社が販売しているCF薬4種類すべてに含まれているCF治療の根幹を成す薬。ただCFの遺伝子変異は1000種類以上存在しており使用できるのはCF患者全体の5~10%。
Lumacaftor:CFTRコレクター
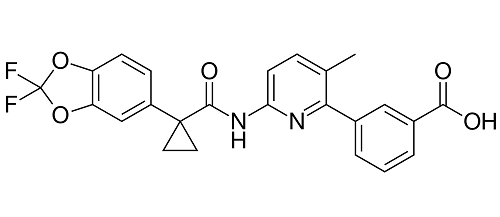
たんぱく質の折り畳み異常であるミスフォールディングにより小胞体関連分解を受けるCFTR Class II変異体の治療に使用される。作用するのはCFTRの生合成中に一時的に存在する中間体。
Lumacaftor単剤では臨床的に有意な治療効果が得られなかったのでCFTRポテンシエーターIvacaftorとの配合薬Orkambiとして使用されている。しかしこの2つの組み合わせは薬物相互作用がありIvacaftorの血中濃度が低下してしまうという問題があった。
tezacaftor:CFTRコレクター
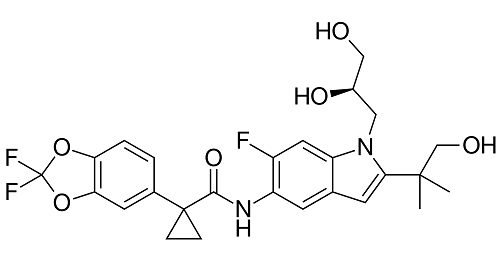
上記の薬物相互作用が起こらないように改善したのがTezacaftorとIvacaftorの配合薬Symdeco。ただ臨床的な効果の差はそれ程でもない。
Elexacaftor:第2世代CFTRコレクター
第1世代CFTRコレクターと作用点が異なりF508 CFTR膜発現を増加させるElexacaftorを含む3成分を合体させたのがVRTX社の大ヒット薬TRIKAFTA。Symdecoは4週間投与により呼吸機能を示す対標準一秒量を7%改善するがTrikaftaは14%改善効果。

TRIKAFTAは守備範囲も広く嚢胞性線維症患者が有する様々なCFTR遺伝子変異に対して約90%をカバーして効果を発揮する。なのでそれまでも3つの薬は使われなくなってきている(VRTXの2022年売り上げの86%)。
このTRIKAFTAの米国内特許は2037年までと長くVRTXのキャッシュフローを力強く支える一番重要な薬。
開発中の薬(2023年8月時点)
| 開発コード | 対象疾患 | 作用機序 | 開発段階 |
| exa-cel | βサラセミア | CRISPR/Cas9 | 3 |
| exa-cel | 鎌状赤血球 | CRISPR/Cas9 | 3 |
| VX-548 | 急性痛 | 電位依存性Na+阻害 | 3 |
| Inaxaplin | APOL1蛋白尿性腎臓病 | APOL1 チャネル阻害 | 3 |
| Vanzacaftor triple | 嚢胞性線維症 | CFTRタンパクプロセシング+移動の正常化 | 3 |
| VX-522 | 嚢胞性線維症 | CFTR mRNA therapy | 1-2 |
| VX-880 | 一型糖尿病 | 膵島細胞療法(門脈経由) | 1/2 |
| VX-264 | 一型糖尿病 | 膵島細胞療法(カプセル化) | 1/2 |
VRTXは2028年までに新薬5つの承認を目指している。
exa-cel
CRISPR Therapeuticsと共同開発している鎌状赤血球症とβサラセミア症の治療薬。CF薬とは違い治療(投与)は一回限りの治療で今流行りのCRISPR/Cas9技術を使用している。効果は既に臨床試験で認められるので今のパイプラインの中では最も承認に近い。
ただ1回で治療が終わる薬は患者にとっては素晴らしくても投資という観点からは好ましくない。なぜなら治療が終わってしまったらもうその薬は売れないから。
exa-celは患者さんにはとても良い治療になると思うのだがVRTXの株価にはそこまで影響しないと思う。
VX-548
アメリカはオキシコドンやフェンタニルといったオピオイド乱用が社会問題となっている。侵襲性が高い手術後だとロキソプロフェンやアセトアミノフェンでは対処できない強い痛みが発生するのでオピオイドは必要な薬ではあるのだが乱用のリスクも高い。
なので非オピオイドで尚且つ痛み止め性能がオピオイド並というVX-548はアメリカで期待されている。作用機序は電位依存性ナトリウムチャネル阻害なので原理的にはリドカインなど麻酔薬に近いのかもしれないがVX-548は経口投与できる点で新しい。
Vanzacaftor triple
3つの成分Vanzacaftor/Tezacaftor/Deutivacaftorを配合したCF薬。CFTRタンパク質のプロセシングおよび輸送の欠陥を改善して細胞表面に正常なCFTRタンパクを発現させる新作用機序をもつ。ただTRIKAFTAが登場したことによりそれまで自社製品のCF薬が使われなくなったように売上的には共食いの可能性がある。mRNA技術を導入しているCF薬のVX-522も。
仮に共食いになっても自社製品なので特許切れ対策にはなるが。TRIKAFTAの特許切れが2037年なのでそれまでに新しいCF薬に患者を移行させておけば2040年くらいまでVRTX社のCF薬フランチャイズは盤石。
VX-880とVX-264
一型糖尿病治療薬。糖尿病にはⅠ型とⅡ型があり暴飲暴食などでなるのはⅡ型。
Ⅰ型は自己免疫疾患などで膵臓β細胞が壊れインスリンが出なくなったりするので治療はインスリンを注射する以外にない。そこで幹細胞由来の膵細胞を注入してインスリン生産を促そうというのがVX-880とVX-264。2つは全く同じ細胞だが違いは形状。
VX-880は門脈経由で投与されるが免疫系が反応してしまうので免疫抑制剤を使用しなければならない。そこでVX-264は細胞をカプセルで包み免疫系から保護しようというアイデア。まだ承認には遠いが開発に成功したら糖尿病治療を根底から変える可能性がある。
糖尿病分野はイーライリリーのマンジャロやノボノルディスクのウゴービの性能が凄すぎてDexcomやInsuletなど糖尿病系テック企業株が暴落しているが一型糖尿病にGLP-1作動薬は効かないのでVX-880とVX-264の成功には関係無い。
