 | |
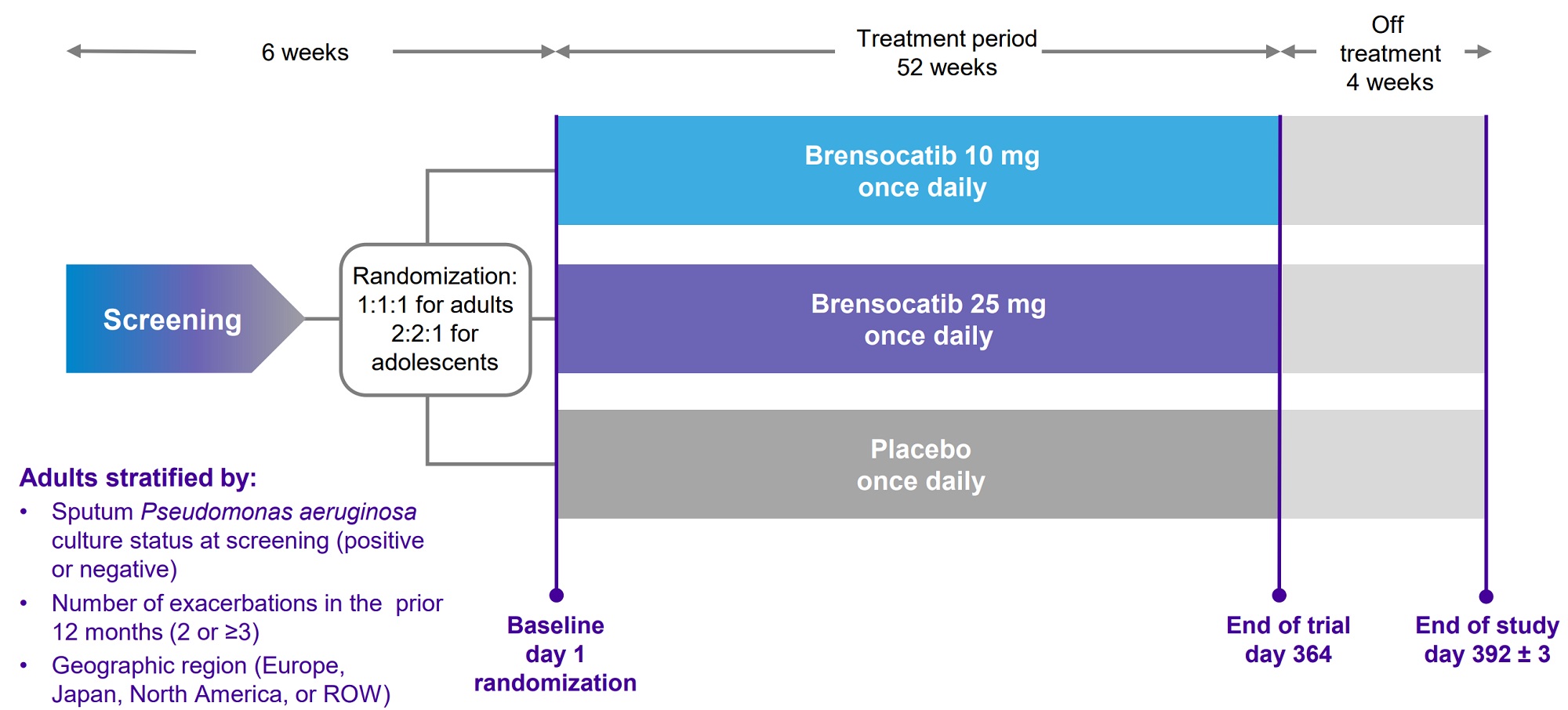
| デザイン | 二重盲検ランダム化プラセボ比較試験 |
| 期間 | 52週間 |
| 対象 | 気管支拡張症 |
| 投与群 | 1. ブレンソカチブ10 mg 2. ブレンソカチブ25 mg 3. プラセボ |
| 主要評価 | 52週間にわたる肺増悪率(年間調整済み) |
| 副次的評価 | 1. 最初の増悪までの時間 |
| 2. 増悪のない患者の割合 | |
| 3. 気管支拡張後FEV1のベースラインからの変化(52週目) | |
| 4. 重度の増悪の年間発生率 | |
| 5. 52週目のQOL-B呼吸器症状ドメインスコアのベースラインからの変化 |
新薬ブレンソカチブ(米インスメッド社)のASPEN試験(フェーズⅢ)結果が発表された。
対象は気管支拡張症。
気管支拡張症は慢性的な気道の炎症を引き起こす疾患の最終段階。
何らかの原因で炎症が起こり気管内の好中球など炎症性メディエーターが過剰放出→エラスチンなどが破壊され不可逆な気管支拡張症が起こる。
気管支拡張症の一般的な症状は慢性の咳、濃厚で粘り気が強い淡。症状が進行すると低酸素血症や肺高血圧症による心不全で呼吸困難となる。
治療はこれまでクラリスロマイシンやアジスロマイシンといったマクロライド系抗生物質の抑制的抗菌薬投与や起動分泌物の除去処置しかなかった。病気の根本にアプローチする治療や薬はこれまで存在しない。
ブレンソカチブは初めてその気管支拡張症の病態の本質にアプローチする薬。
炎症が起こっている部位では好中球セリンプロテアーゼが過剰に生産されていて、それが炎症の原因となっている。
そのセリンプロテアーゼを活性化するのがジペプチジルペプチダーゼ-1(DPP1)。なのでそのDPP-1を阻害するブレンソカチブは気管支拡張症を改善する可能性がある。
気管支拡張症の患者は米国で約45万人、欧州で約40万人、日本で約15万人の患者が罹患していて承認されたら一番最初にアクセスできる薬となる。
インスメッドはブレンソカチブの販売申請を2024年Q4にFDAへ提出する予定、米国内で2025年半ばに発売する予定となっている。
日本では2026年の上半期に販売予定。
承認されたら年間売上高は最大40億ドルを超えると予想。
| ブレンソカチブ(10mg) | ブレンソカチブ(25mg) | プラセボ | |
| n | 583 | 575 | 563 |
| 年齢(平均) | 59.8 ± 15.9 | 60.6 ± 15.8 | 60.0 ± 15.4 |
| 75歳以上, n (%) | 83 (14.2) | 84 (14.6) | 93 (16.5) |
| 女性, n (%) | 385 (66.0) | 360 (62.6) | 362 (64.3) |
| 白人, n (%) | 431 (73.9) | 430 (74.8) | 405 (71.9) |
| BMI | 25.5 ± 5.4 | 25.4 ± 5.1 | 25.1 ± 4.9 |
| 慢性抗生物質使用(%) | 146 (25.0) | 154 (26.8) | 133 (23.6) |
| マクロライド | 110 (18.9) | 114 (19.8) | 105 (18.7) |
| 吸入ステロイド使用(%) | 324 (55.6) | 324 (56.3) | 352 (62.5) |
| 緑膿菌 (%) | 203 (34.8) | 205 (35.7) | 199 (35.3) |
| 過去12ヶ月間に3回以上の増悪(%) | 172 (29.5) | 163 (28.3) | 167 (29.7) |
| BSI, 平均 (標準偏差) | 7.1 (3.5) | 7.1 (3.6) | 7.1 (3.6) |
| 気管支拡張薬投与後の予測FEV1 %, | 74.3 (23.4) | 74.3 (24.6) | 71.9 (22.2) |
| 血中好酸球数 ≥300 cells/μL, n (%) | 115 (19.7) | 111 (19.3) | 106 (18.8) |
| COPD既往歴, n (%) | 77 (13.2) | 83 (14.4) | 102 (18.1) |
| 喘息既往歴, n (%) | 101 (17.3) | 109 (19.0) | 111 (19.7) |
| 喫煙歴, n (%) | 164 (28.1) | 163 (28.3) | 183 (32.5) |
| QOL-B RSS (成人), | 59.8 (17.0) | 61.9 (17.2) | 60.0 (16.8) |
参加者の平均年齢は60歳、白人が7割だが日本や韓国でも行われたのでアジア人も参加している。
3人中2人は女性、抗生物質の使用は4人中1人、でそのうち8割はクラリスロマイシンかアジスロマイシンを使用。半数以上は吸入ステロイド薬を使用。重症化の因子である緑膿菌感染は3人中1人。
| 適格基準 | 除外基準 |
| 気管支拡張症と一致する | COPDまたは喘息の一次診断(二次診断は可) |
| CTによる気管支拡張症の確認 | 嚢胞性線維症による気管支拡張症 |
| 気管支拡張薬投与後のFEV₁が予測値の30%以上 | 既知または疑われる免疫不全障害 |
| 成人:18歳から85歳 | ABPA、結核、または非結核性抗酸菌症の治療中 |
| 青少年:12歳以上18歳未満 | 1日12時間を超える補助酸素使用 |
| 成人:BMI 18.5 kg/m²以上 青少年:体重30 kg以上 | 喫煙者 |
| 成人:12ヶ月間に2回以上の増悪 青少年:12ヶ月間に1回以上の増悪 | 全身性ステロイド or 免疫調節剤の使用 |
| 来院時に喀痰サンプルを提供できる |
年齢は12歳から85歳までの気管支拡張症患者が参加。
除外基準はまずタバコ吸っている人。プレドニンとかネオーラルのように免疫を強力に押さえつける内服薬を使用してる人も参加不可能。
酸素吸入に生活の半分以上を依存している重傷者も参加不可。
嚢胞性線維症による気管支拡張症患者には別のアプローチが可能なので除外。
| 肺増悪率(52週間・年間調整済み) |
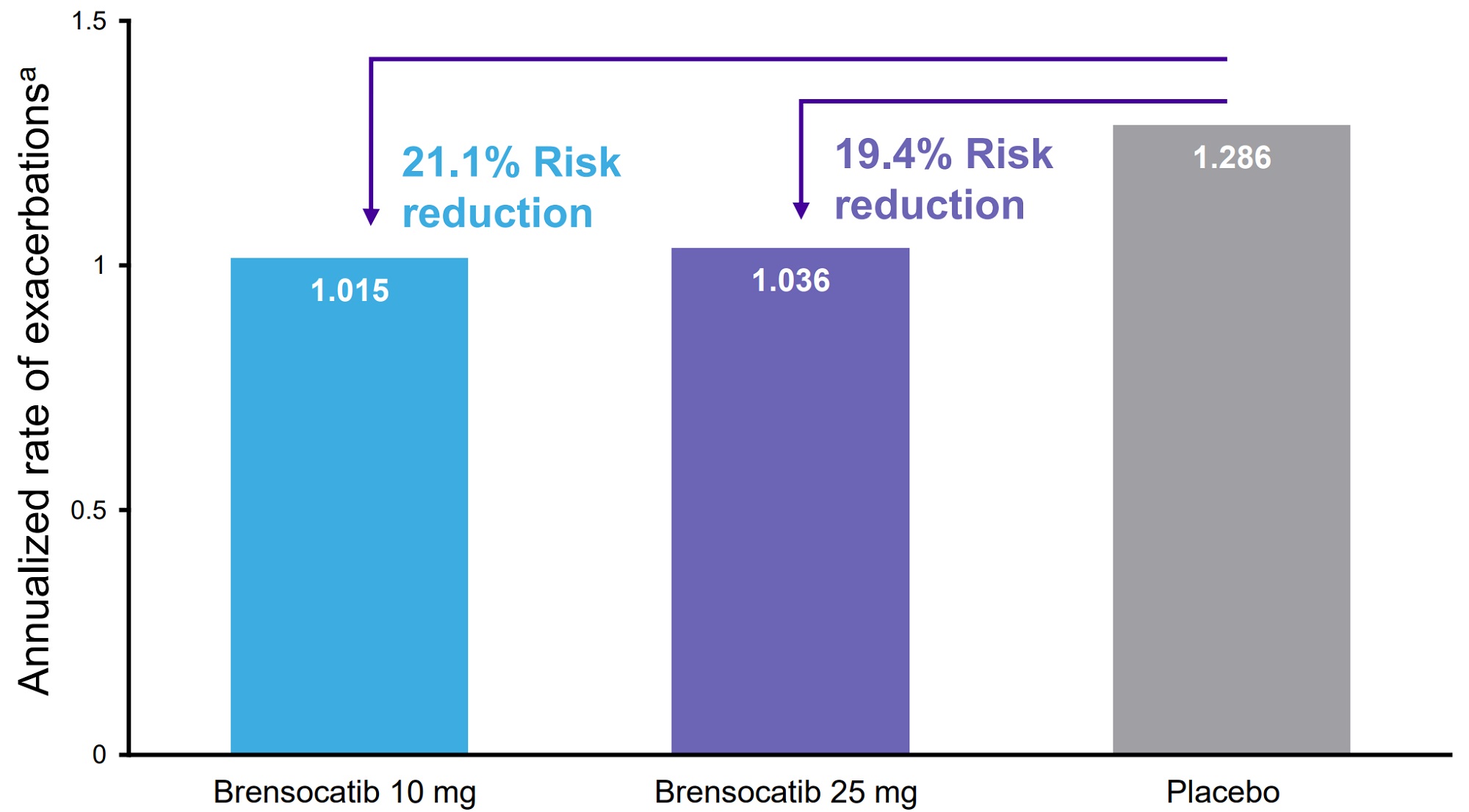 |
ブレンソカチブ10mg、ブレンソカチブ25mgをプラセボ対象に行った二重盲検比較試験。
主要評価項目である肺増悪率はプラセボと対比してブレンソカチブ10mg群も25mg群もリスクを約20%低下させた(統計学的に有意な減少)。
この主要評価項目だと用量が多くても少なくても効果が変わらない。
| 最初の肺疾患増悪発生までの期間延長 |
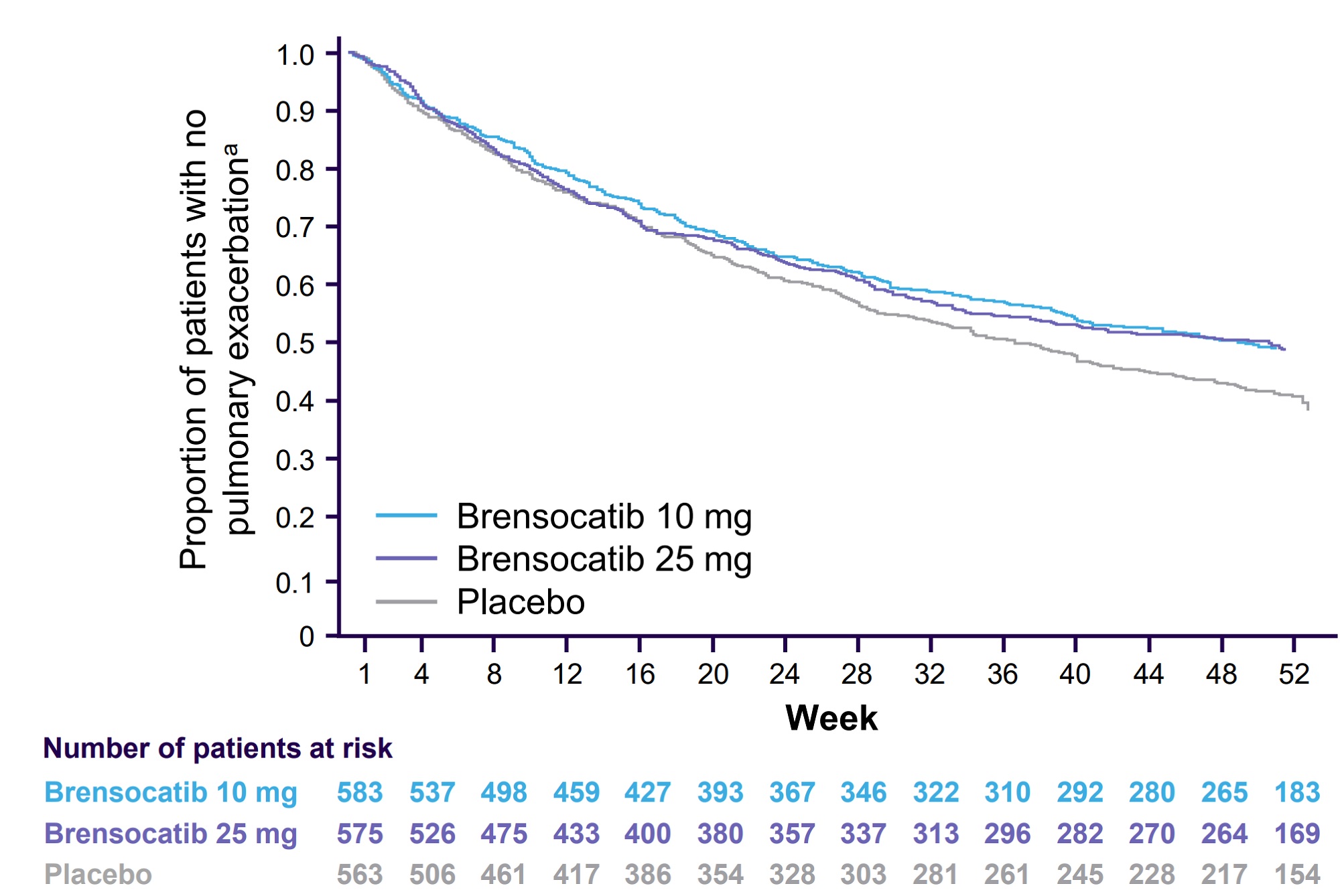 |
半分の患者が増悪するまでの期間を両群ともプラセボに対して約2割ほど延長している。これもブレンソカチブ群同士では差が無い。
| 気管支拡張薬投与後の1秒量(FEV1)のBLからの変化 |
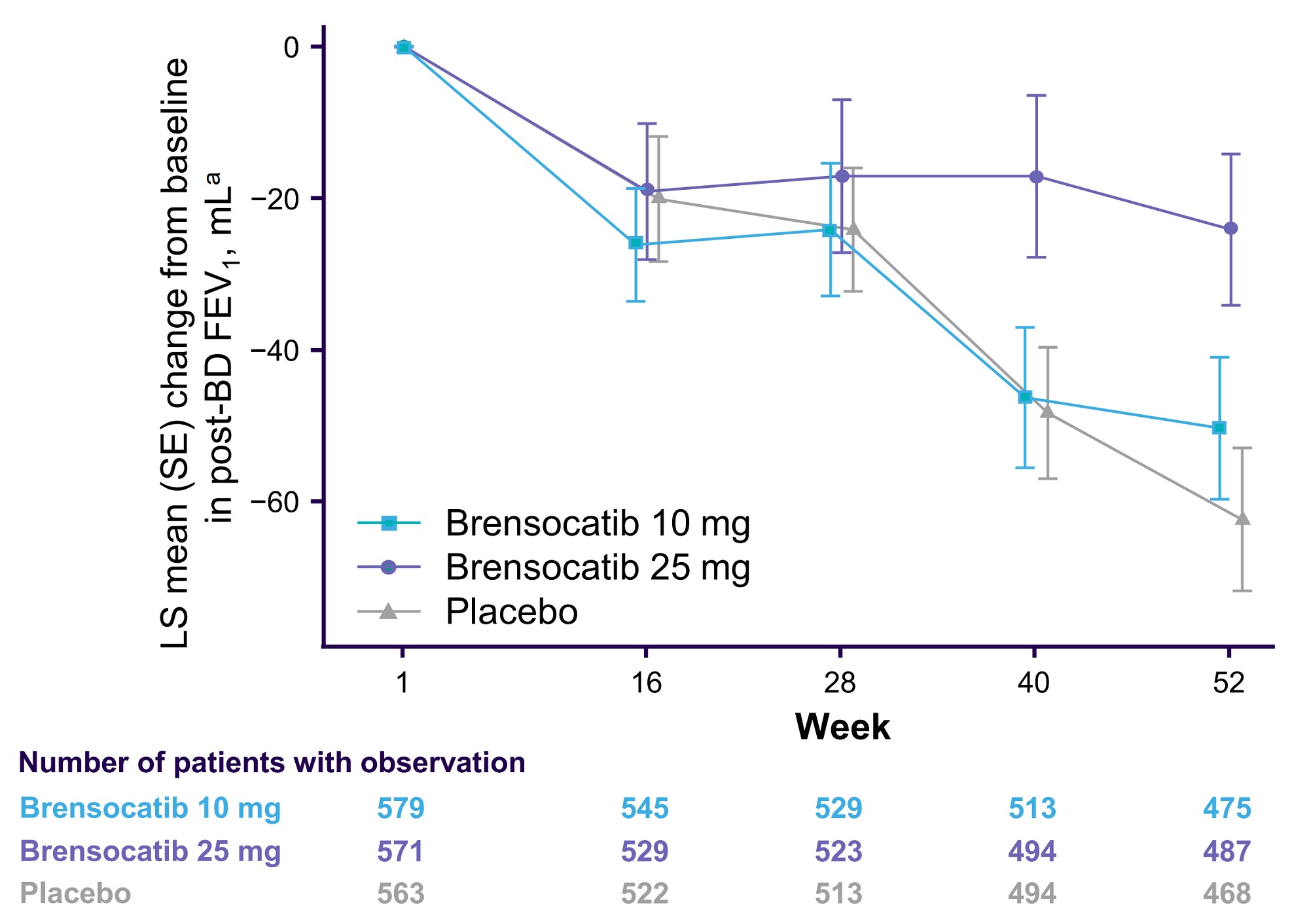 |
1秒量の変化はブレンソカチブ10mgとブレンソカチブ25mgで大きな差が出た。
ブレンソカチブ10mgはプラセボに対して11mLの増加、だが25mg群は38mLと統計的に有意な違い。
| 気管支拡張症(QOL-B)の呼吸器スコアのBLからの変化 |
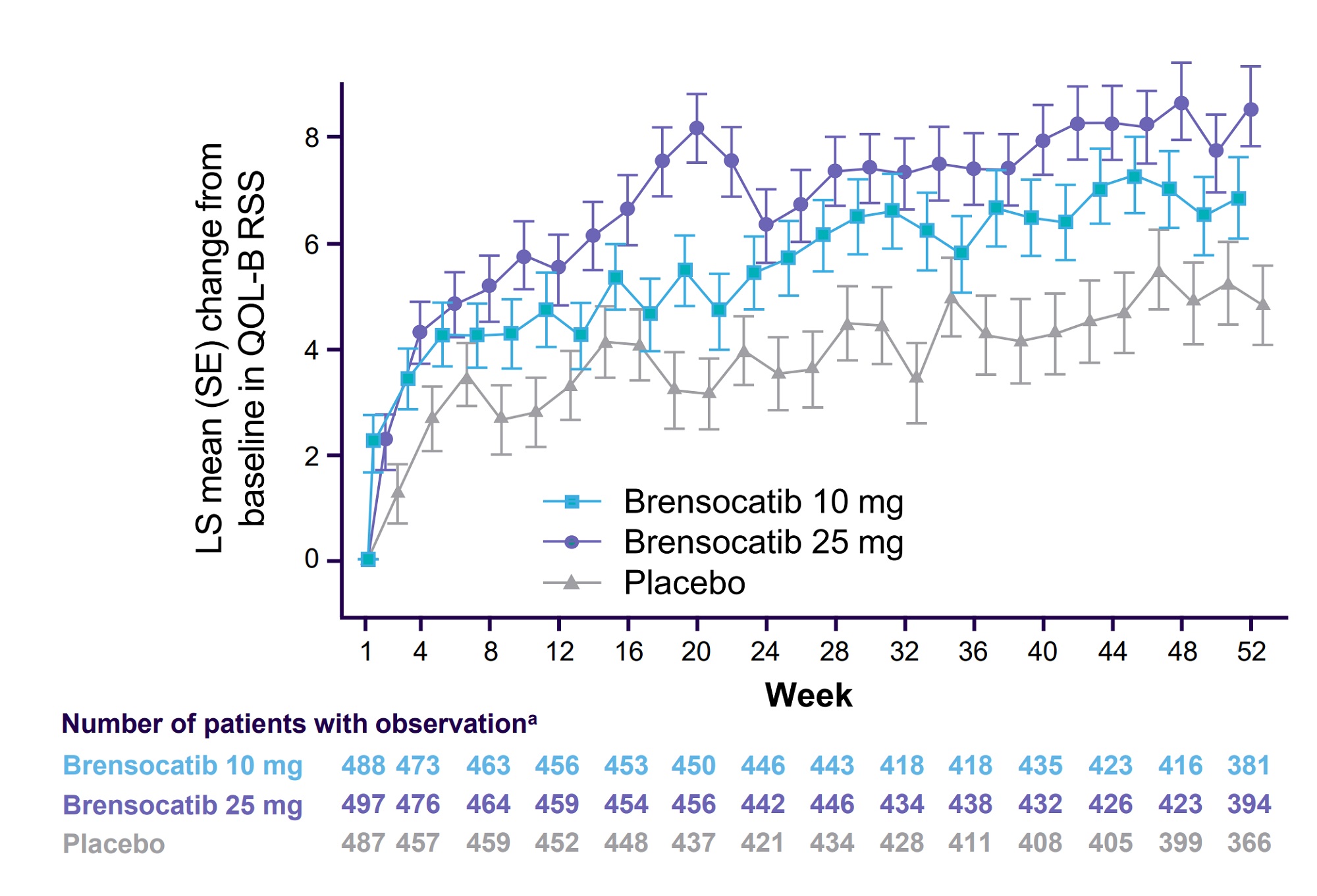 |
呼吸器スコアの変化はブレンソカチブ25mg>ブレンソカチブ10mg>プラセボの順に綺麗なグラフとなった。
服用開始の一か月後には効果を実感し始めてそれから緩やかに1年を通してスコアは上昇している。少なくとも1年間は効果が低下したりすることはなさそう。
| (AE) の発生件数, n (%) | ブレンソカチブ25mg | ブレンソカチブ10mg | プラセボ |
|---|---|---|---|
| 全てのAE | 440 (76.7%) | 452 (77.7%) | 448 (79.6%) |
| 重篤なAE | 101 (17.4%) | 97 (16.9%) | 108 (19.2%) |
| 治療に関連するAE | 72 (12.4%) | 85 (14.8%) | 73 (13.0%) |
| 重篤な治療関連AE | 0 | 1 (0.2%) | 0 |
| 治療による死亡 | 3 (0.5%) | 4 (0.7%) | 7 (1.2%) |
| 治療中止に至るAE | 25 (4.3%) | 22 (3.8%) | 23 (4.1%) |
| 試験中止に至るAE | 14 (2.4%) | 16 (2.8%) | 16 (2.8%) |
両群ともプラセボと比べて有害事象が明らかに増加するような事は無し。
| 注目すべきAE | Brensocatib 10 mg | Brensocatib 25 mg | プラセボ |
|---|---|---|---|
| COVID-19 | 92 (15.8%) | 120 (20.9%) | 89 (15.8%) |
| 鼻咽頭炎 | 45 (7.7%) | 36 (6.3%) | 43 (7.6%) |
| 咳 | 41 (7.0%) | 35 (6.1%) | 36 (6.4%) |
| 頭痛 | 39 (6.7%) | 49 (8.5%) | 39 (6.9%) |
注目すべき有害事象としてはCOVID-19感染が25mg群で少しだけプラセボと比較して高い。それ以外は特にプラセボより明らかに増加したAEは無し。
| 特別な関心のあるAE, | Brensocatib 10 mg | Brensocatib 25 mg | プラセボ |
|---|---|---|---|
| Any AE | 42 (7.2) | 56 (9.8) | 53 (9.4) |
| 角化症 | 8 (1.4) | 17 (3.0) | 4 (0.7) |
| 歯周炎/歯肉炎 | 8 (1.4) | 12 (2.1) | 15 (2.7) |
| 重篤な感染症 | 4 (0.7) | 7 (1.2) | 4 (0.7) |
| 肺炎 | 23 (4.0) | 27 (4.7) | 33 (5.9) |
ブレンソカチブが作用するDPP1の別名をカテプシンCと言う。
このカテプシンC遺伝子に生まれつき異常があるとパピヨン・ルフェーブル症候群(常染色体劣性遺伝)という稀な病気になる。掌蹠角化症や重度の歯周炎が起こり乳歯と永久歯の両方が早期に脱落したりする。
ブレンソカチブはDPP1=カテプシンCを阻害する薬なのでパピヨン・ルフェーブル症候群に類似した副作用が出るのではと心配されていた。
角化症が発生率高めだが歯周炎や歯肉炎はプラセボよりも低くパピヨン・ルフェーブル症候群に関連するAEは無さそう。
ブレンソカチブは、FDA から画期的治療薬指定(Breakthrough Therapy Designation)を受けており順調にいけば気管支拡張症治療薬として初めて米国や日本で承認される。
一番最初に市場にアクセスできる薬が売り上げも一番期待できる。DPP4阻害薬の効果はどれも大きな違いはないが一番最初に登場したジャヌビアが一番売れている。薬も半導体も先頭を切っている会社が一番儲かる。
じゃあ気管支拡張症治療薬を一番最初に世に送り出すインスメッド株はこれからバーテックス株のように右肩上がりなのかはまだ分からない。
インスメッド社は2024年8月時点で承認された薬を一つだけしかない。アリケイスという吸入薬。
このアリケイスも1日用バイアルが38,000円で年間1000万円を超える超高額な薬なのだが使う人が少ないのでそこまで売上が期待できない。
2023年のアリケイス売上は3億ドル。
アリケイスだけを考えるとピーク時の売上10億ドル辺りと予想されているので現在のインスメッドの時価総額130億ドルは超割高。
なのでインスメッド株はブレンソカチブの成功にかかっている。
時価総額130億ドルでもアリケイスとブレンソカチブが年間50億ドルを売り上げたら割安となる。
そのためにはブレンソカチブは今回の試験で証明した気管支拡張症だけでなく、現在試験進行中である慢性副鼻腔炎での成功も必要となる。